FDA-Freigaben zeigen: Medizinisches Titan wird zur regulatorischen Beweiskette
Zwei jüngste FDA 510(k)-Freigaben verweisen auf eine praktische Verschiebung für Lieferanten von medizinischem Titan: Der Markt fragt nicht mehr nur, ob aus Titan ein Implantat gefertigt werden kann. Er fragt, ob die Titan-Route durch Designkontrolle, Fertigungsvalidierung, Prüfung, Sterilisation und regulatorische Freigabe lückenlos dokumentiert werden kann.

Das erste Signal ist EASYMADE-TI von CG Bio. Die 510(k)-Datenbank der FDA listet das Gerät als vorgeformte, nicht veränderbare Kranioplastik-Platte unter K252251 mit einer Entscheidung zur wesentlichen Gleichwertigkeit vom 9. April 2026 und einem Seiten-Update am 4. Mai (FDA). CGBIO erklärte, das patientenspezifische Titan-Implantat werde aus individuellen CT-Daten für die kraniale und nicht lasttragende kraniofaziale Rekonstruktion entworfen, mittels Laser Powder Bed Fusion aus medizinischem Titan gefertigt und nach der Designarbeit in Korea an US-Krankenhäuser geliefert (CGBIO über PR Newswire).
Das zweite Signal ist das PC Fix-System von Chest Wall Innovations. Die FDA listet K260411 als Knochenfixationsplatte von Chest Wall Innovations mit einer Entscheidung zur wesentlichen Gleichwertigkeit vom 24. April 2026 (FDA). Das Unternehmen erklärte, das Rippenfixationssystem biete sowohl PEEK- als auch Titan-Implantate und unterstütze intrathorakale und extrathorakale chirurgische Zugänge (Chest Wall Innovations über PR Newswire).
Keine der beiden Freigaben sollte als breite Prognose für die Titan-Nachfrage gelesen werden. Geräte-Freigaben sind produktspezifisch, und die Pressemitteilungen der Unternehmen geben weder Werkstoffspezifikationen noch Mengen oder Lieferketten preis. Die nutzbare Branchenlektion ist enger, aber stärker: Medizinisches Titan wird als Teil einer regulierten Beweiskette bewertet, nicht als generische Metallkategorie. Dasselbe Muster zeigt sich in benachbarten Segmenten — siehe unsere Analysen zur Qualifizierungskette für Luftfahrt-Titan und zum TITAN-AM-Nachweisrahmen für additive Fertigung.
Warum 510(k)-Freigaben für Werkstofflieferanten zählen
Im 510(k)-Überblick der FDA heißt es, dass Hersteller eine Vorvermarktungs-Mitteilung einreichen müssen, bevor bestimmte Geräte in den kommerziellen Vertrieb eingeführt werden, und bevor wesentliche Änderungen vorgenommen werden, die Sicherheit oder Wirksamkeit beeinflussen können. Die FDA bezieht in diese Diskussion ausdrücklich Änderungen an Design, Material, chemischer Zusammensetzung, Fertigungsprozess und Indikationen für die Anwendung ein (FDA).
Diese Formulierung ist für Titan-Verarbeiter wichtig. Ein Lieferant denkt vielleicht in Kategorien von Güteklasse, Form und Preis: Stab, Platte, Blech, Bearbeitungsrohling, Implantatplatte, Pulver oder Fertigteil. Ein Geräteunternehmen denkt darüber nach, ob dieses Material in einer regulierten Produktakte verteidigt werden kann. Dieselbe Legierungsbezeichnung kann je nach Pulverhistorie, Schmelzroute, Sauerstoffkontrolle, Bearbeitungskontamination, Oberflächenzustand, Prüfprotokoll, Reinigungsprozess und Verpackungs-Workflow sehr unterschiedliche Risiken bergen.
Bei konventionellem medizinischem Titan beginnt die Beweiskette in der Regel mit chemischer Zusammensetzung und mechanischen Eigenschaften. Bei additiv gefertigtem Titan erweitert sie sich um Pulverqualität, Wiederverwendungskontrollen, Prozessparameter, Nachbearbeitung, Maßprüfung, Oberflächeneigenschaften und Validierungsnachweise. Bei patientenspezifischen Implantaten kommen Designdaten und ein fallspezifischer Workflow hinzu. Ein Material, das im Lager akzeptabel aussieht, kann dennoch ungeeignet sein, wenn die Aufzeichnungen ihm nicht in die Geräte-Historie folgen können.
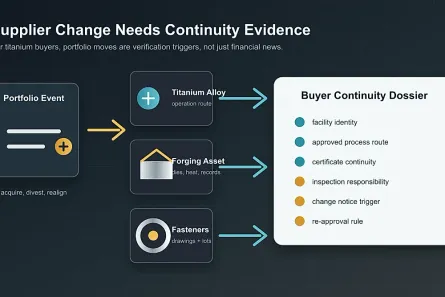
Die neue Beweiskette für medizinisches Titan
Das klarste Rahmenwerk für Einkäufer ist:
| Beweis-Tor | Was rückverfolgbar sein muss | Warum es zählt |
|---|---|---|
| Werkstoffspezifikation | Legierung, Güteklasse, Chemie, mechanische Daten und Chargenidentität | Die Geräteakte braucht mehr als ein kommerzielles Werkstoff-Label |
| Fertigungsroute | Stab, Platte, Bearbeitung, LPBF, poröse Struktur, Wärmebehandlung oder Endbearbeitung | Die Route beeinflusst Wiederholbarkeit, Oberflächenzustand und Validierungsaufwand |
| Designkontroll-Akte | Patientenspezifisches Modell, Implantatgeometrie, Indikation und Prädikat-Logik | Die Geräte-Freigabe hängt von Verwendungszweck und Designvergleich ab |
| Prüfung und Validierung | Maßprüfungen, mechanische Prüfung, Prozessvalidierung und Abweichungslenkung | Medizinische Einkäufer brauchen Aufzeichnungen, die einem Audit standhalten |
| Sterilisations- oder Krankenhaus-Workflow | Sauberkeit, Verpackung, Sterilisationsverantwortung und Liefer-Timing | Ein fertiges Implantat ist nicht einsetzbar, bis der klinische Workflow es annehmen kann |
| Regulatorische Eignung | 510(k), Prädikat-Gerät, Produktcode und Indikationen für die Anwendung | Die regulatorische Freigabe ist an das spezifische Gerät und den Anwendungsfall gebunden |

Das bedeutet nicht, dass jeder Lieferant von Titan-Halbzeugen zum Hersteller fertiger Geräte werden muss. Es bedeutet, dass Lieferanten, die medizinische Kunden bedienen, verstehen sollten, an welcher Stelle ihr Werkstoffnachweis in die Akte des Kunden eingeht. Ein Titanstab für die Bearbeitung von Wirbelsäulen- oder Trauma-Komponenten, ein Plattenrohling für die kraniale Rekonstruktion und Ti-6Al-4V ELI-Pulver für LPBF-Implantate stehen jeweils unterschiedlichen Dokumentationsfragen gegenüber.
LPBF verändert das Lieferantengespräch
EASYMADE-TI ist besonders nützlich, weil es zeigt, wie additive Fertigung das Käufergespräch verändert. Das Unternehmen beschreibt einen Prozess, in dem CT-Daten des Patienten zu einem maßgeschneiderten Design führen, LPBF das Titan-Implantat produziert und das Produkt zur Krankenhaus-Sterilisation und -Anwendung geliefert wird. In diesem Workflow verkauft der Titan-Lieferant nicht mehr nur einen Werkstoff-Input. Die Materialroute berührt Design, Geometrie, Prozess-Wiederholbarkeit, Reinigung, Prüfung und Logistik.
Für Lieferanten von Titan-Pulver erhöht dies die Nachweis-Hürde. Käufer können nach Partikelgrößenverteilung, Chemie, Fließverhalten, Sauerstoffaufnahme, Pulverhandhabung und Wiederverwendungsrichtlinie fragen. Für Bearbeitungslieferanten umfassen die entsprechenden Fragen Chargenrückverfolgung, Kühlmittelkontrolle, Gratentfernung, Oberflächengüte und Prüfprotokolle. Für Platten- oder Stab-Lieferanten kann der Schwerpunkt auf Güteklassen-Konformität, Ultraschallprüfung, mechanischen Prüfungen und sauberer Verpackung liegen.
Der gemeinsame Faden ist, dass medizinisches Titan dokumentationsreif sein muss, bevor es produktreif ist.
Titan konkurriert auch nach Anwendungsfall
Die PC Fix-Freigabe fügt eine zweite Lektion hinzu: Titan ist nicht immer die einzige Werkstoff-Geschichte. Chest Wall Innovations hebt ein System hervor, das sowohl PEEK- als auch Titan-Implantate enthält. Das ist relevant, weil die Werkstoffwahl bei Medizingeräten oft ein Kompromiss zwischen Festigkeit, Steifigkeit, Bildgebungsverhalten, chirurgischem Zugang und klinischem Anwendungsfall ist.
Für Titan-Lieferanten sollte die Schlussfolgerung nicht sein, dass Titan automatisch gewinnt. Die bessere Schlussfolgerung lautet: Titan muss durch die richtigen Nachweise für die richtige Indikation gestützt werden. Wenn starre Fixierung, Haltbarkeit oder etablierter orthopädischer Einsatz wichtig ist, kann Gr.5 / Gr.23 Ti-6Al-4V ELI attraktiv sein. Wenn Bildgebungssichtbarkeit oder Elastizität eine stärkere Designanforderung ist, können alternative Werkstoffe in Betracht gezogen werden. Der Lieferant, der die Rolle von Titan im Anwendungsfall des Geräts erklären kann, wird glaubwürdiger sein als der Lieferant, der Biokompatibilität als vollständiges Verkaufsargument behandelt.
Was exportierende Titan-Lieferanten vorbereiten sollten
Exportlieferanten, die medizinische Kunden bedienen, sollten ihre Dokumentation rund um den regulierten Workflow des Kunden aufbauen, nicht rund um einen generischen Produktkatalog. Die nützliche Frage lautet nicht: „Haben wir Titan in medizinischer Güte?” Sie lautet: „Kann unsere Titan-Akte ohne Lücken in das Design-, Validierungs- und Regulierungssystem eines Geräteherstellers eingefügt werden?”
Das bedeutet klare Chargenrückverfolgung, stabile Werkstoffspezifikationen, Prüfberichte passend zum geforderten Standard, dokumentierte Prozesshistorie, kontrollierte Endbearbeitung über Lohnzerspanung, Prüfprotokolle, Kontaminationskontrollen und realistische Lieferzeiten. Für die LPBF-bezogene Versorgung wird der Pulverhandhabungsnachweis zentral. Für bearbeitete oder plattenbasierte Implantate zählen Oberflächenzustand, Maßkontrolle und Reinigungsrouten stärker.
Die jüngsten FDA-Freigaben beweisen keinen plötzlichen Boom bei jedem medizinischen Titan-Produkt. Sie zeigen aber, warum sich der hochwertige Teil des Marktes in Richtung nachweisreicher Versorgung bewegt. Bei Medizingeräten ist Titan nicht nur ein Metall, das sich im Körper bewährt. Es ist ein Werkstoff, der über Design, Fertigung, Validierung und regulatorische Prüfung rückverfolgbar bleiben muss. Lieferanten, die diese Kette unterstützen können, werden für ernsthafte Medizingerätekäufer leichter zu qualifizieren sein.
Verwandte Produkte und Dienstleistungen
- Spezielle Titan-Legierungen (Gr.5 / Gr.23 / Ti-6Al-4V ELI) — Referenz in medizinischer Güte nach ASTM F136 / ISO 5832-3
- Titanstab / Titanrundstange — Bearbeitungsmaterial für Wirbelsäulen-, Trauma- und kraniale Komponenten, ASTM B348-Rückverfolgbarkeit
- Titanblech und -platte — Plattenrohlinge für Kranioplastik und Knochenfixation
- Titan-Schmiedeteile — endkonturnahe Schmiederohlinge für orthopädische und Trauma-Anwendungen
- Titandraht — Ausgangsmaterial für AM- und chirurgische Drahtanwendungen
- Lohnzerspanungs-Dienstleistungen — Endbearbeitung, Maßprüfung, kontrollierte Endbearbeitungs-Lieferung für Implantatrohlinge
- Titan-Branchennachrichten — laufende Verfolgung von Qualifizierungsketten für medizinisches, Luftfahrt- und Chemie-Titan
FAQ
# Warum braucht medizinisches Titan mehr als eine reine Legierungsklassifizierung?
# Was ist eine Beweiskette für medizinisches Titan?
# Wie verändert LPBF die Anforderungen an Lieferanten von Titan-Implantaten?
# Beweist eine FDA 510(k)-Freigabe, dass ein Titan-Implantat klinisch überlegen ist?
# Worauf sollten exportierende Titan-Lieferanten für Medizingerätekäufer vorbereitet sein?
Benötigen Sie dieses Material? Erhalten Sie ein Direktangebot ab Werk.